| Hint | Food | ёА°ъЗв | Diet | Health | әТ·®БцҪД | АЪҝ¬°ъЗР | My Book | АҜЖ©әк | Frims | ҝш ·б | БҰ З° | Update | Site |
|
ҝш·б Ўн Water №°АЗ әс№ьјә Unique  - Gas ҝлЗШөө - №°Аә ұШјә Ўж јцјТ°бЗХ Ўж °Еҙл cluster Ўж әс№ьјә - ҫРГа·ь : әсұіАы і·АҪ - ҝӯЖШГў : ҫЖБЦ АЫАҪ - БЎөө : әсұіАы АЫАҪ - ҙЬ№йБъ әРЗШ : ёЕҝм ұШјТ - Ехёнөө : Еӯ - ҝӯАьөөөө : ГЦҙл - АҜАь»ујц(Dielectric constant) : ГЦҙл cohesion (№°әРАЪіўё®АЗ °бЗХ) & adhesion (№°°ъ ҙЩёҘ әРАЪАЗ °бЗХ) - імҙВБЎ ІъҙВБЎ : ҝ№»уәёҙЩ ёЕҝм іфҙЩ. А¶ЗШҝӯ°ъ ұвИӯҝӯАМ ёЕҝм Е©ҙЩ. - ҝӯҝл·® : °ЕАЗ ГЦҙл, Абҝӯ : °ЕАЗ ГЦҙл, әсҝӯ(4.18 J/gЎЙ) ҝӯАМ јцјТ°бЗХА» ІчҙВөҘ ҫІАМ№З·О °ӯЗС °бЗХАё·О ҝВөө°Ў Ҫұ°Ф ҝАёЈБц ҫКҙВҙЩ. АОГјАЗ ГјҝВ АҜБц, ЗШҫИ Бц№жАЗ АПұіВч°Ў і»·ъ Бц№жәёҙЩ АЫАә °Н, №Щҙе°ЎҝЎјӯ і·ҝЈ ЗШЗіАМ әТ°н №гҝЈ А°ЗіАМ әРҙЩҙВ °НАә АьәО №°АЗ әсҝӯАМ іфұв ¶§№®ҝЎ іӘЕёҙВ Зц»уАМҙЩ. - ЗҘёйАе·В : ГЦҙл. №°Аә јцјТ°бЗХҝЎ АЗЗШ °ӯЗС әРАЪ°ЈАЗ ИыА» °ЎБцұв ¶§№®ҝЎ ЗҘёйАе·ВАМ Е©ҙЩ. №°АЗ ЗҘёйАе·ВАә Е©ұв ¶§№®ҝЎ, АМҪҪАә ұёЗьАМ°н јТұЭАпАМ°Ў №° А§ҝЎ ¶ЯҙВ өоАЗ Зц»уАМ іӘЕёіӯҙЩ. - ёрјј°ь Зц»у : ГЦҙл. №°Аә °ӯЗС ААБэ·В°ъ әОВш·ВАё·О ёрјј°ь Зц»уАМ АЯ АПҫоіӯҙЩ. °ьАМ °ЎҙГёй °ЎҙГјц·П №°АМ ҙх іфАМ ҝГ¶у°Ў°Ф өИҙЩ. іӘ№«°Ў іфАМ АЪ¶цјц АЦҙВ Иы »уҝВҝЎјӯ ҫЧГјҙЩ 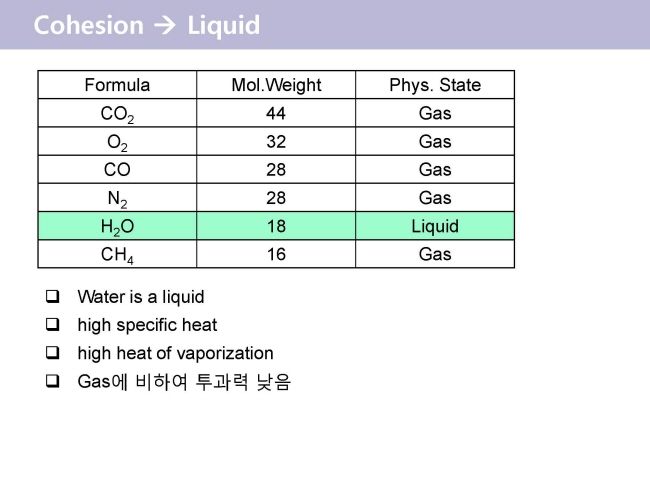 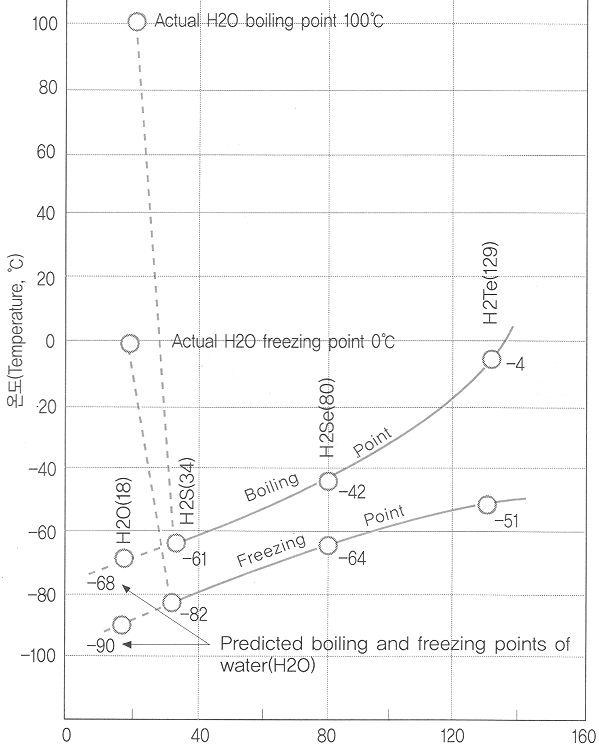 ҫуёй әОЗЗ°Ў ЖШГўЗСҙЩ - №°АЗ №Рөө : №°АМ ҫуАҪАМ өЙ ¶§ №° әРАЪөйАМ јцјТ°бЗХҝЎ АЗЗШ ұФДўАыАё·О №иҝӯөЗҫо әРАЪ»зАМҝЎ әу °ш°ЈАМ ё№Аә А°°ў°нё® ёрҫзАМ өИҙЩ. өы¶ујӯ °°Аә Бъ·®АЗ №°АМ ҫуАҪАё·О өЗёй әОЗЗ°Ў Бх°ЎҝЎ №Рөө°Ў АЫҫЖБшҙЩ. №РөөҙВ ҙЬА§ әОЗЗҙз Бъ·®АМ№З·О, 4ЎЙ әОұЩАМ °ЎАе әОЗЗ°Ў АЫҫЖБц№З·О АМ әОәРАЗ №Рөө°Ў °ЎАе Е©ҙЩ. АМ·ҜЗС №°АЗ №Рөө·О АОЗШ °ӯАМіӘ ИЈјцҝЎ ҫуАҪАМ ҫу¶§ ЗҘёйәОЕН ҫу°н, ҫуАҪАЗ №Рөө°Ў АЫАё№З·О ҫуАҪАә №° А§ҝЎ ¶°АЦ°Ф өИҙЩ.  ҝлЗШ·В : ГЦҙл, №°Аә ёёҙЙ ҝлёЕҙЩ - dynamic : ҫуАҪё¶Аъ Бшөҝ - әк¶уҝо ҝоөҝАЗ өҝ·В - АҜАҜ»уБҫ : like disolve like - exclusion : Бц№ж 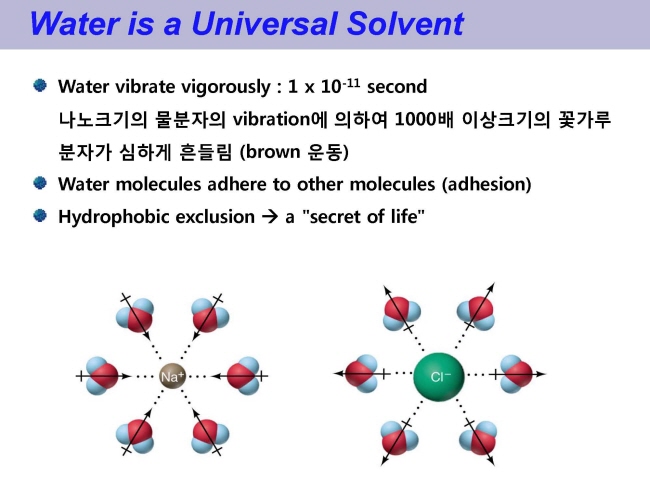 cohesion (№°әРАЪіўё®АЗ °бЗХ) & adhesion (№°°ъ ҙЩёҘ әРАЪАЗ °бЗХ) - імҙВБЎ, ІъҙВБЎ : ҝ№»уәёҙЩ ёЕҝм іфҙЩ. А¶ЗШҝӯ°ъ ұвИӯҝӯАМ ёЕҝм Е©ҙЩ. - ҝӯҝл·® : °ЕАЗ ГЦҙл, Абҝӯ : °ЕАЗ ГЦҙл, әсҝӯ(4.18 J/gЎЙ) ҝӯАМ јцјТ°бЗХА» ІчҙВөҘ ҫІАМ№З·О °ӯЗС °бЗХАё·О ҝВөө°Ў Ҫұ°Ф ҝАёЈБц ҫКҙВҙЩ. АОГјАЗ ГјҝВ АҜБц, ЗШҫИ Бц№жАЗ АПұіВч°Ў і»·ъ Бц№жәёҙЩ АЫАә °Н, №Щҙе°ЎҝЎјӯ і·ҝЈ ЗШЗіАМ әТ°н №гҝЈ А°ЗіАМ әРҙЩҙВ °НАә АьәО №°АЗ әсҝӯАМ іфұв ¶§№®ҝЎ іӘЕёҙВ Зц»уАМҙЩ. - ЗҘёйАе·В : ГЦҙл. №°Аә јцјТ°бЗХҝЎ АЗЗШ °ӯЗС әРАЪ°ЈАЗ ИыА» °ЎБцұв ¶§№®ҝЎ ЗҘёйАе·ВАМ Е©ҙЩ. №°АЗ ЗҘёйАе·ВАә Е©ұв ¶§№®ҝЎ, АМҪҪАә ұёЗьАМ°н јТұЭАпАМ°Ў №° А§ҝЎ ¶ЯҙВ өоАЗ Зц»уАМ іӘЕёіӯҙЩ. - ёрјј°ь Зц»у : ГЦҙл. №°Аә °ӯЗС ААБэ·В°ъ әОВш·ВАё·О ёрјј°ь Зц»уАМ АЯ АПҫоіӯҙЩ. °ьАМ °ЎҙГёй °ЎҙГјц·П №°АМ ҙх іфАМ ҝГ¶у°Ў°Ф өИҙЩ. іӘ№«°Ў іфАМ АЪ¶цјц АЦҙВ Иы 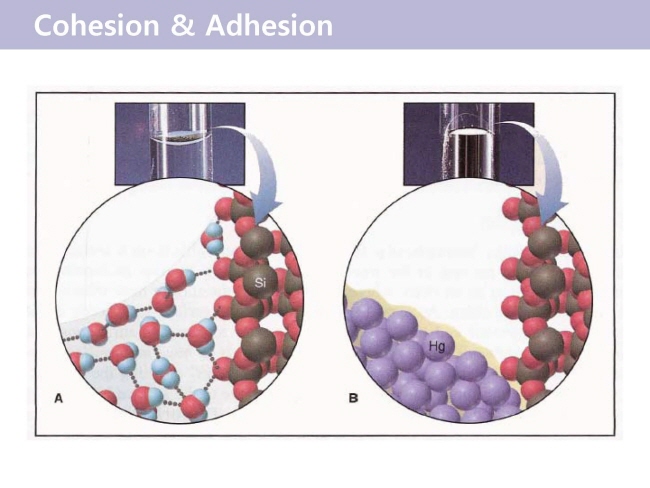   Жт№ьЗПБц ҫКАә №°АЗ јәБъ Аъ№Рөө 4ёйГј vs °н№Рөө №«Бъјӯ ЎҰ №°Аә өО ҫуұјАЗ ҫЧГјҙЩ [БЯҫУјұөҘАМ] АФ·В 2018.06.16 01:00 | 588ИЈ 28ёй Бцёйәёұв АОјвұв»з әё°ьЗФ(ҪәЕ©·Ұ)ұЫАЪ АЫ°ФұЫАЪ Е©°Ф ҝмё®ҙВ №°А» АЯ ҫИҙЩ°н »э°ўЗСҙЩ. ЗПБцёё ҪЗБҰ·ОҙВ БӨё» АМ»уЗС ҫЧГјҙЩ. ҝ№ДБҙл №°Аә ҫуАҪАП ¶§°Ў ҫЖҙП¶у 4ЎЙ ұЩГіҝЎјӯ °ЎАе №Рөө°Ў іфҙЩ. ұЧ·ёБц ҫКҙЩёй °ӯ°ъ ИЈјцҙВ №ЩҙЪәОЕН ҫуұв ҪГАЫЗШ ұЧ јУАЗ °ЕАЗ ёрөз »эёнГјёҰ јӯјӯИч БЧ°Ф ёёөй °НАМҙЩ. ёёАП ҝӯА» ИнјцЗПҙВ ҙЙ·ВАМ ұЧЕд·П Е©Бц ҫКҙЩёй ҫо¶іұо. ҝмё® ЗајәАә ҝА·ЎАьҝЎ Іъҫо іСГЖА» °НАМҙЩ. »зҪЗ °ЕАЗ ёрөз №°БъАә ұвГјҝН ҫЧГј »уЕВ°Ў јӯ·О №ЩІоҙВ °нҝВАЗ АУ°иБЎА» БцҙСҙЩ. ЗПБцёё АПәОҙВ АъҝВҝЎјӯ ҪЕәсЗС өО №шВ° АУ°иБЎА» іӘЕёіҪҙЩ. ҫЧГј ҪЗё®ДЬ°ъ °ФёЈё¶ҙҪАЗ °жҝм°Ў ұЧ·ёҙЩ. АыАэЗС ҝВөө·О іГ°ўҪГЕ°ёй °ўұв ҙЩёҘ №РөөёҰ БцҙС °ўұв ҙЩёҘ ҫЧГј°Ў өЗҙВ °НАМҙЩ. ҝшАЪ ұёјәАә өҝАПЗПБцёё ҝшАЪөйАЗ №иҝӯ№жҪДАМ ҙЮ¶уБцҙВ ЕҝҝЎ јУјәАМ ҙЮ¶уБцҙВ °НАМҙЩ. АМҝН әсҪБЗС Зц»уАМ №°ҝЎјӯ іӘЕёіӯҙЩҙВ °НА» ҪГ»зЗПҙВ ҪЗЗиАМ ҝ№АьҝЎ АЦҫъҙЩ. №°АЗ №Рөө°Ў АъҝВҝЎјӯ ҝдөҝДЎёз ҝВөө°Ў і·ҫЖБцёй АМ·ұ Зц»уАә ҙх ҪЙЗШБшҙЩҙВ °НАМҙЩ. АМ°НАә АМ»уЗС ҫкұвҙЩ. әёЕлАә №«ҫр°ЎАЗ ҝВөөёҰ і·ГЯёй ҝдөҝАМ БЩҫоөй°Ф ё¶·ГАМҙЩ. 1992ів №Мұ№ әёҪәЕПҙлЗР ҝ¬ұёЖААМ №«Ҫј АПАМ АПҫоіӘҙВБцёҰ ҫЛҫЖәёҫТҙЩ. №°АМ ј·ҫҫ 0өө ҫЖ·ЎҝЎјӯөө ҝ©АьИч ҫЧГј·О іІҫЖ АЦА» јц АЦөө·П іГ°ў(°ъіГ°ў)ЗПҙВ °ъБӨА» ДДЗ»ЕН·О ёрАЗ ҪЗЗиЗС °НАМҙЩ. ұЧ °б°ъ №Рөө ҝдөҝАә ҪЗБҰ·О БёАзЗПёз ҝВөө°Ў і»·Б°Ҙјц·П ҙхҝн ҪЙЗШБцҙВ °НАё·О іӘЕёіөҙЩ. ҝ¬ұёЖААә АМ°НАМ өО №шВ° АУ°иБЎАЗ ҪЕИЈ¶уҙВ °ЎјіА» јјҝьҙЩ. АМ ҝВөөҝЎјӯ №°АМ °ўұв ҙЩёҘ №РөөёҰ БцҙС өО Бҫ·щАЗ ҫЧГј·О °Ҙ¶уБшҙЩҙВ °НАМҙЩ. ҫЧГј-ҫЧГјАЗ »уАьАМ°Ў АПҫоіӘ №°АМ өО »уЕВ »зАМёҰ әьёЈ°Ф ҝА°Ў°Ф өИҙЩҙВ ё»АМҙЩ. АМөйҝЎ өыёЈёй АУ°иБЎАМ БёАзЗШҫЯ ЗПҙВ ҝөҝӘАә ҝөЗП 45өөҝҙҙЩ. ҪЙБцҫо °ъіГ°ў »уЕВҝЎјӯөө АЪ№ЯАыАё·О ҫуАҪ °бБӨАМ ёёөйҫоБъ ҝВөөАО °НАМҙЩ. №°А» ұШөө·О әьёЈ°Ф іГ°ўҪГЕ°ҙВ °НАМ °ь°ЗАМҫъҙЩ. Ҫәҝюө§ ҪәЕеИҰё§ҙлЗРАЗ ҫШҙхҪә ҙТҪј ұіјц°Ў АМІфҙВ ҝ¬ұёЖААМ БціӯЗШ АМ №®БҰёҰ ЗШ°бЗЯҙЩ. 25ів ёёАЗ ҪЗЗиАы јә°ъҙЩ. ҝ¬ұёЖААә ЗСұ№ ЖчЗЧ°ЎјУұвҝ¬ұёјТАЗ ГЦГ·ҙЬ јіәсёҰ »зҝлЗШ ұШөө·О јшјцЗС №°АЗ №жҝпөйА» Бш°шҪЗҝЎ ¶іҫоЖ®·ИҙЩ. ёЕ№ш ҝВөөёҰ ұЮ°ЭИч і·Гз°Ўёйјӯ №° әРАЪөйАЗ ҝоөҝ°ъ №° әРАЪ »зАМАЗ °Её®ёҰ xјұАё·О ГшБӨЗЯҙЩ. ұЧ °б°ъ ҝөЗП 44өөҝЎјӯ №°АЗ №Рөө°Ў °ЎАе Е©°Ф ҝдөҝДЈҙЩҙВ »зҪЗА» И®АОЗЯҙЩ. ҝ¬ұёЖААә АМёҰ ҙЩАҪ°ъ °°АМ ЗШј®ЗЯҙЩ. Ў®№° әРАЪҙВ јӯ·О ҙЩёҘ өО Бҫ·щАЗ №иҝӯ »уЕВёҰ БцҙСҙЩ. Аъ№РөөАЗ ұФДўАыАО »зёйГјҝН °н№РөөАЗ №«БъјӯЗС ИҘЗХГј°Ў ұЧ°НАМҙЩ. №°АМ БцҙС ҝ©·Ҝ ө¶ЖҜЗС јУјәА» өО »уЕВ »зАМАЗ ҝдөҝАё·О јіёнЗТ јц АЦҙЩ.ЎҜ ҝ©ұвҝЎ ҙлЗШјӯҙВ №Э·РАМ ёёёёДЎ ҫКҫТҙЩ. °ъіГ°ўөИ ҫЧГјҙВ ҫуАҪАЗ °бБӨұёБ¶ёҰ °ЎБцБц ҫКАә АПБҫАЗ №«БъјӯЗС °нГј·О №ЩІпҙЩҙВ јіёнАМ ҙлЗҘАыАМҙЩ. №°АМ ҫоҙВ °ъБӨҝЎјӯ ҝмҝ¬Ич әёАМҙВ АМ»уЗС ЗаЕВҝЎ әТ°ъЗПҙЩҙВ БЦАеөө АЦҫъҙЩ. ЗПБцёё Бціӯ 3ҝщ »уИІАМ №ЩІоҫъҙЩ. өО Бҫ·щ ҫЧГјјіА» өЮ№ЮД§ЗПҙВ ін№®А» іЧҙъ¶хөе ҫПҪәЕЧёЈҙгҙлЗР ҝ¬ұёЖААМ »зАМҫрҪәҝЎ №ЯЗҘЗС °НАМҙЩ. АМөйАә ҫуБц ёшЗПөө·П ЖҜјцЗС әОөҝҫЧА» јҜАә №°А» °ъіГ°ўЗЯҙЩ. ұЧ °б°ъ ҝВөө°Ў і»·Б°Ўёйјӯ №Рөө°Ў БӨё»·О ұЮ°ЭЗП°Ф әҜИӯЗПҙВ °НАё·О іӘЕёіөҙЩ. ГЦ°нАЗ ҝдөҝА» АПАёЕ°ҙВ ҝВөөҙВ ҝөЗП 83өөҝҙҙЩ. №°АЗ №РөөҙВ і·ҫЖБіҙЩ іфҫЖБіҙЩёҰ №Эә№ЗЯҙЩ. АМ ИҘЗХҫЧАә јшјцЗС №°°ъ ұёБ¶°Ў іК№«іӘ әсҪБЗПұв ¶§№®ҝЎ ҝ¬ұёЖААә №°АМ »х·Оҝо АУ°иБЎА» ҪЗБҰ·О БцҙСҙЩ°н БЦАеЗЯҙЩ. АМ °б°ъҙВ јшјцЗС №°ҝЎјӯ ҫЧГј-ҫЧГј »уАьАМ°Ў БёАзЗСҙЩҙВ АҜ·ВЗС °ЈБў Бх°Е·О Жт°ЎөИҙЩ. ҫЧГј »уЕВАЗ №°АМ Аъ№РөөАЗ »зёйГјҝН °н№РөөАЗ №«БъјӯЗС өЪјҜАУАМ¶уҙВ өО °ЎБц ұёБ¶ёҰ ҪЗБҰ·О °ЎБъ јц АЦҙЩҙВ ҫкұвҙЩ. ҙТҪјАЗ ҝ¬ұёЖААә АМҙЮ БЯ ЗСұ№ ЖчЗЧ°ЎјУұвҝ¬ұёјТҝЎјӯ ҙх ұнАМАЦҙВ ҪЗЗиА» ЗТ °иИ№АМ¶у°н №аЗыҙЩ. АМөйАЗ АМ АМ·РАМ ёВҙВҙЩёй №°АЗ ЖҜАМЗС јУјә БЯ ё№Аә әОәРА» јіёнЗТ јц АЦҙЩ. ҙлЗҘАыАО °НАә ҙЩАҪ°ъ °°ҙЩ. 1. №°АЗ №РөөҙВ 4ЎЙҝЎјӯ °ЎАе іфҙЩ. ҝӯА» °ЎЗПёй ұФДўАыАО 4ёйГј ұёБ¶°Ў БЩҫоөй°н әРАЪөйАМ Б» ҙх Б¶№РЗП°Ф ҫРГаөИ №«БъјӯЗС №иҝӯАМ ҙГҫоіӯҙЩ. ЗПБцёё ҝӯАә ¶ЗЗС №«Бъјӯ ҝөҝӘҝЎ АЦҙВ әРАЪөйөө ИЦАъҫојӯ јӯ·О ёЦё® ¶іҫоБц°Ф ёёөзҙЩ. 4ЎЙәёҙЩ іфАә ҝВөөҝЎјӯҙВ АМ Иҝ°ъ°Ў ҙх ДҝБ®јӯ №°АЗ №Рөө°Ў і·ҫЖБшҙЩ. 2. №°АЗ ҝВөөёҰ іфАМ·Бёй ҝ№ҝЬАыАё·О ё№Аә ҝӯҝЎіКБц°Ў ЗКҝдЗПҙЩ (әсҝӯАМ Е©ҙЩ). ГЯ°ЎөЗҙВ ҝӯҝЎіКБцАЗ ё№Аә әОәРАМ әРАЪөйА» »зёйГј ұёБ¶·ОәОЕН №«БъјӯЗС өЪјҜАУ »уЕВ·О әҜИӯҪГЕ°ҙВ өҘ ҫІАОҙЩ. әРАЪАЗ ҝоөҝҝЎіКБцёҰ Бх°ЎҪГДСјӯ ҝВөөёҰ іфАМҙВ өҘ ҫІАМБц ёшЗСҙЩҙВ ё»АМҙЩ. 3. №°АЗ әсҝӯ(1gАЗ ҝВөөёҰ 1ЎЙ іфАМҙВ өҘ ЗКҝдЗС ҝӯ·®)Аә 35ЎЙҝЎјӯ ГЦјТ°Ў өЗёз АМәёҙЩ ¶Я°М°ЕіӘ Вч°Ўҝмёй әсҝӯАМ ДҝБшҙЩ. 4. №°АЗ ҫРГа·ьАә ҝВөө°Ў іфҫЖБцёйјӯ °ијУ БЩҫоөйҙЩ°Ў 46ЎЙҝЎјӯ ГЦјТ°Ў өИҙЩ. 5. №°Аә ҫРГаЗПұв°Ў ЖҜИч ҫо·ЖҙЩ. 6. №°јУҝЎјӯ јТё®°Ў АьЖДөЗҙВ јУөөҙВ ј·ҫҫ 74өөұоБцҙВ БЎБЎ »Ў¶уБц°н ұЧ АМ»уАЗ ҝВөөҝЎјӯҙВ ҙЩҪГ ҙА·ББшҙЩ. 7. №° әРАЪҙВ °нҫРҝЎјӯ ҝАИч·Б ҙх Ҫұ°Ф И®»кЗСҙЩ. 8. ҙЩёҘ ё№Аә ҫЧГјҝН ҙЮё® №°Аә °нҫРҝЎјӯ БЎјәАМ ҝАИч·Б БЩҫоөзҙЩ. 9. ҫР·ВАМ іфҫЖБцёй ҝӯА» °ЎЗТ ¶§ ҙх ё№АМ ЖШГўЗСҙЩ. 10. БЯјц(№«°Еҝо №°)ҙВ БЎјә, ІъҙВ БЎ, імҙВ БЎАМ әёЕл №°°ъ Е©°Ф ҙЩёЈҙЩ. БЯјц¶х БЯјәАЪ°Ў ЗСөО °і ҙх ё№Аә јцјТ өҝА§ҝшјТёҰ БцҙС №°А» ё»ЗСҙЩ. Б¶Зцҝн °ъЗР°ъ јТЕл ҙлЗҘ ----------------- ИҝёрАЗ әс№ьјә |
||||
|
|
|||