식품 ≫ 기호성 ≫ Flavor
향료 : 물리적 성질, 분자 구조
향료 물질의 물리,화학적 특성
휘발성을 가진다 : 분자량 : 26 ~ 300 이하, 비등점 : 120 ~350'C
비 중 : 1.0 전후
굴절율 : 1.5 전후
성 상 : 대부분 액상, 일부 수지상, 결정상
용해성 : 물과 기름에 어느 정도 용해성이 있어야 한다
어느 정도 수용성 이어야 코 점막의 수층을 통하여 수용기로 도달하고
어느 정도 지용성 이어야 신경세포의 세포막에 들어갈 수 있다
관능기 또는 불포화 결합을 가지고 있다
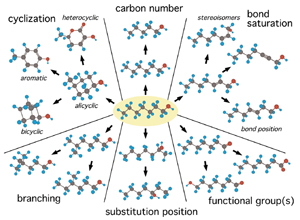
향이 있는 물질은 반드시 휘발성이 있고 약간의 친수성과 상당한 친유성이 있어야 한다. 따라서 향료물질은 대부분 분자량이 300이하(보통 200)이하의 탄소수 16개 이하(4~16개)다. 그중에서 8~10개의 범위가 가장 우아한 방향을 가지고 탄소수가 적으면 짧고 강하고 길어지면 미묘하고 오래가는 향취가 된다. 따라서 전체 유기물 중 향기물질은 40~50 만종 정도로 추정한다. 이중 인간이 산업적으로 사용하는 것은 식품이 2500종 이하 향장품등 전체를 합해도 5000종이하다
1. 우리들의 코는 일반적으로 20문자 이하의 짧은 단어를 좋아한다. 예를 들어 O=C1CCCCCCCCCCCCCCC1은 무스크 냄새를 내는데, 이것보다 C가 단지 두 문자 더 긴O=C1CCCCCCCCCCCCCCCCC1은 냄새가 없다. 대체적으로 말하면 C가 16개 이상인 분자는 냄새가 없을 가능성이 높다. 더 큰 분자들은 우리의 후각 메커니즘에 맞지 않는다.
2. 단어가 짧을수록 냄새도 짧게 지속된다. CSC를 피부에 뿌리면 30초 동안 트뤼플 냄새가 난다. 이것은 향료 세계에서 ‘톱노트(top note)’라 알려져 있다. 대체로 문자 한 개가 증가하면 시간이 두배로 늘어난다. CC(C)=CCCC(C)=CC=O를 뿌려보면 30분 전도 동안 레몬 냄새가 난다. 이것은 콜롱(cologne)과 같은 향수의 ‘하드노트(heart note)가 된다’ 그러나 CC1CC(C)(C)C2CC(C)=C(C=C2C1(C)C)C(C)=O를 뿌리면 값싼 무스크 냄새가 30시간 또는 그 이상 지속된다. 이것은 “바텀노트(bottom note)가 된다.
3. 냄새 분자는 몇 개의 예외를 제외하면 불과 다섯 종류의 원자로 되어있다.(예외의 하나는 지나치게 화려한 히야신스와 같은 냄새를 내는 브로모스틴렌(bromostyrene)으로, 크고 억센 브롬(Br)을 포함하고 있는데 지금은 사용되고 있지 않다.)다섯 개란 탄소, 수소, 산소, 질소, 황(C,H,O,N,S)이다. 이 원소들은 모두 주기율표의 같은 쪽, 즉 오른 쪽 윗부분에 있다. 놀랍게도 이들은 모든 생명체를 구성하는 다섯 원소이기도 하기 때문에 이것은 당연하다고도 말할 수 있다.
4. 냄새 분자는 공간을 날아 코에 도달해야 하기 때문에 서로를 들러붙게 하는 전하를 가지고 있지 않아야 한다((+)도 (-)도 아니다). 단어의 말단에 –O와 같은 너무 많은 점착성 그룹을 가지지 않아야 한다. 냄새 분자는 ‘수소결합(hydrogen bond)’이라는 약한 결합으로 서로 결합되어 있고 그 결합이 분자들을 날아가지 못하게 한다.
5. 원료는 가능한 비활성인 것이어야 한다. OO나OOO(페록시화합물이나 오존화합물)또는 N=NC(디아조화합물)과 같은 재미있는 것이나 ONC(이소시아네이트), NCS(티오시아네이트)등과 같이 반응성이 높은 것은 팔 생각은 안하는 것이 좋다.
6. 같은 냄새가 나는 두 단어는 없다. 예를 들어 O=C1CCCCCCCCCCCCC1은 무스크 냄새가 나는데, C가 한 개 적은 O=C1CCCCCCCCCCCC1은 시더우드 냄새가 난다. 냄새에는 형제처럼 비슷한 것이 많이 있지만 완전히 똑 같은 쌍둥이는 없다. 어떻게 그렇게 확신할 수 있는가? 향료 화학자들에게 물어보면 알겠지만 지금까지 수를 헤아릴 수 없을 정도의 분자, 즉 다른 단어들이 만들어져 왔다. 그렇다면 그것들을 두개씩 비교해 보면 된다. 결코 같은 냄새는 없을 것이다
화학 구조에 따라 분자에 인력이 영향을 주어 물리적 성질을 다르게 만든다. 따라서 용액에서 향료의 증발 속도 및 보유력(fixation)에 영향을 주어 향의 성질이 용매나 베이스에 따라 달라지는 이유를 설명할 수 있다.
1) 휘발성
향의 인지는 분자가 코에 들어가 물리적으로 후각 수용 뉴런과 결합해 이루어진다. 이것은 향이 증기 상태로 되어 있을 때 인지가 가능하다는 것을 의미한다. 향의 증발 과정은 향료에서 중요하며 향기의 휘발성은 향의 특성에서 중요하다. 사실상 몇몇의 조향사는 휘발성에 기초한 향수 조합 방법을 제시했다.
일반적으로 큰 분자는 휘발성이 낮고 작은 분자는 휘발성이 높다. 예를 들어 모노테르펜은 세스퀴테르펜(sesquiterpene)에 비해 휘발성이 높 덜 지속적이다. 그러나 산소를 포함한 작용기를 가진 분자의 경우는 휘발성이 낮아지며 그 예로는 에탄(ethane), 벤젠은 에틸알코올, 벤질알코올에 비해 휘발성이 높다. 분자가 작을수록 작용기의 효과는 더욱 영향을 받는다. 히드록시 시트로넬랄과 같이 한 개의 분자에 2개의 작용기가 있는 경우 더욱 더 휘발성을 낮춘다.
산소를 포함한 작용기가 휘발성을 낮추는 이유는 전자 전하의 편극에 기인한다. 극성을 가진 분자는 서로 끌리며 그렇기에 서로 떨어지지 못하도록 하여 휘발성을 낮춘다. 편극의 정도는 각 작용기에 따라 다르다. 예를 들어 C=O를 가진 알데히드, 케톤, 에스테르는 수소결합을 가진 hydroxyl (-OH)가 있는 산이나 알코올보다 약하게 끌린다. 알코올에서 이런 물질은 약하게 연결된 체인 구조(chain structure)를 이루고 카르복실 그룹(carboxylic group)을 만든다. 편극과 수소결합은 향수의 보유력에 있어 아주 중요한 역할을 하며 극성 효과는 GC의 분리에 있어 중요하다.
에스테르의 휘발성은 숙지해야 한다. 에스테르는 알코올과 산(acid)으로 결합되어 있어 결과적으로 약한 극성 카르복실그룹(polarizing carboxylic group)을 갖고 있다. 그러므로 에스테르는 알코올과 산보다 휘발성이 좋다. 그러나 에스테르의 크기는 모분자들 보다 더욱 휘발성에 영향을 준다.
예를 들어 에틸페닐아세테이트(Ethyl phenylacetate)는 분자 크기는 크나 페닐아세트산(phenylacetic acid)보다 더 큰 휘발성을 갖는다. 유사하게 페닐에틸 아세테이트는 약간 더 페닐에틸알코올보다 휘발성이 좋다. 그러나 페닐에틸페닐아세테이트(phenylethyl phenylacetate)는 페닐에틸알코올보다 훨씬 더 휘발성이 약하고 페닐아세트산보다도 약한 휘발성이 있다. 이것은 구조와 연관되어 있다. 비록 에스테르가 산소에 붙은 산(acid)처럼 카르보닐 그룹을 갖고 있더라도 2번째 산소는 다른 탄소와 붙어 있다. 이런 결합은 에스테르 성질에 있어 무극성(nonpolar)이 되어 휘발성에 영향을 주지 않는다. 그렇기에 에테르인 페닐에틸메틸에테르(phenylethyl methyl ether)와 이소아밀에테르(iso-amyl ether)는 페닐에틸 알코올에 비해 많은 탄소로 구성되나 훨씬 휘발성이 좋다. 로즈 옥사이드(rose oxide)는 모노테르펜의 유도체이나 휘발성이 좋다. 왜냐하면 극성(polar)작용기인 피란 고리(pyran ring)를 갖고 있기 때문이다. 매우 큰 분자인 갈락소라이드(galaxolide)는 작용기를 갖고 있지 않음에도 불구하고 분자 크기로 인해 지속성이 매우 좋다. 결론적으로 큰 분자는 작은 분자보다 지속성이 좋고 이런 성질은 작용기의 존재에 따라 달라질 수 있다. 이는 작용기의 편극화와 수소결합 때문이며 같은 크기에서 하이드로카본(hydrocarbone)과 에테르는 알데히드, 케톤, 에스테르보다 더욱 휘발성이 좋다.
2)용해도
분자간 인력은 용해도에 영향을 준다. 서로 다른 용매에서 용해도는 분자내, 분자간 인력의 관계에 따라 달라진다. 만약에 용매와 용질의 분자내, 분자간 인력이 같다면 용해도는 높으나 다를 경우 용해도는 낮아진다. 이 의미는 극성 용매는 극성 용질에 있어 좋은 용매이고 비극성 용매는 좋지 않은 용매임을 뜻한다.
작용기에 있어 극성은 비극성 탄소가 증가함에 따라 감소한다. 혼합 용매의 경우 각각 용매들의 합의 중간에 있다. 향료에서 점도를 증가시키기 위해 염을 넣어 주는데 이는 물의 극성을 증가시키고 향료의 용해성를 낮춘다. 수용성향의 용해성 문제는 낮은 온도에서 문제가 되고 유화 시스템은 높은 온도에서 문제가 된다. 그러나 다중상(multiple phase : 에멀전, 비누)에서는 용해도 문제가 없다. 또한 향료와 용매의 강한 결합은 향료의 증발 속도를 감소시켜 향의 강도를 낮춘다. 향은 여러 원료의 혼합물이기에 용해된 용매에 따라 향이 다를 수 있다. 결과적으로 향료의 강도는 향료 베이스에 따라 그리고 향료끼리의 물리적 작용에 따라 영향을 받을 수 있다.
3)지속성
향료의 지속성은 휘발성에 달려 있다. 그러나 향료의 농도 및 향료와 베이스와의 인력도 영향을 준다. 예를 들어 시향지에 적용할 때 10%는 1% 알코올보다 더욱 지속성이 있고, 같은 1% 라도 용매가 휘발성 용매인 에틸 알코올(Ethyl alcohol)과 비휘발성인 용매에 희석된 경우 향료가 인력에 의해 더욱 지속성이 높아진다. 약한 향의 경우 향료가 비휘발성 용매에 있을 때 향을 거의 느낄 수 없게 만들 수 있다. 그러나 알코올의 증발에 있어 쌍극자 모멘트(dipole moment)또는 수소결합이 향료의 증발 속도를 낮출 수 있다. 조향사들은 증발 속도가 큰 향료의 증발 속도를 낮추기 위해 낮은 휘발성의 향료를 사용하는데 이를 보류제(fixative)이라 한다.