| Hint | Food | 맛과향 | Diet | Health | 불량지식 | 자연과학 | My Book | 유튜브 | Frims | 원 료 | 제 품 | Update | Site |
|
내몸 ≫ Control ≫ 신경전달물질 신경전달 물질 : γ-Aminobutyric acid (GABA) 신경전달물질 : 신경전달물질 종류 - 글루탐산의 역할 Glu : 흥분 - 운동 : 아세틸콜린, 니코틴 생리작용 - 흥분 : Glu, Aspartate, 글리신 - 억제 : GABA - 감정 : 트립토판 - 세로토닌, 멜라토닌 - 감정 : 티로신 - 도파민, 노르아드네날린, 아드네날린 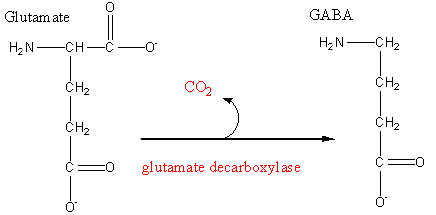  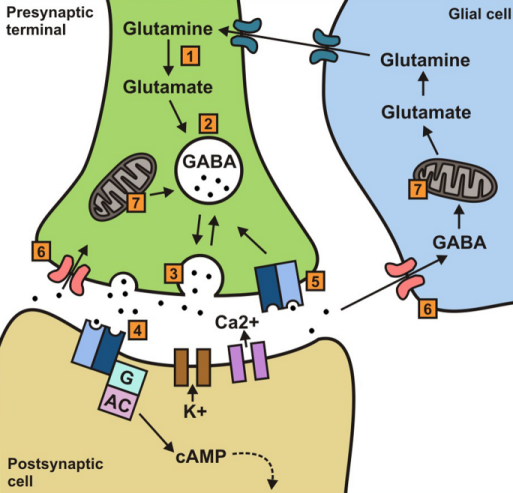 브레이크 적용 : chief inhibitory neurotransmitter in the mammalian central nervous system. 뉴론의 1만개 시냅스중 8000개 정도가 glutamic acid 수용체, 2000개 gaba 수용체 GABA의 신경 전달 물질과 수용체는 다양한 뇌 기능에 관여하고 있습니다. GABA의 불균형은 또한 양극성 장애, 정신 분열증, 그리고 불안 장애와 관련이 있다. GABA의 주요 기능은 신경세포의 발화 억제이기 때문에 GABA는 신체를 ‘안정시키는’ 지시에서 중요한 역할을 담당한다.따라서 GABA시스템은 과도한 자극으로부터 뇌를 보호하는 일종의 정보 필터 역할을 한다. In vertebrates, GABA acts at inhibitory synapses in the brain by binding to specific transmembrane receptors in the plasma membrane of both pre- and postsynaptic neuronal processes. This binding causes the opening of ion channels to allow the flow of either negatively charged chloride ions into the cell or positively charged potassium ions out of the cell. Depending on which ion channels open, the membrane potential is either hyperpolarized or depolarized. This action results in a negative change in the transmembrane potential, usually causing hyperpolarization. Two general classes of GABA receptor are known: GABAA in which the receptor is part of a ligand-gated ion channel complex, and GABAB metabotropic receptors, which are G protein-coupled receptors that open or close ion channels via intermediaries (G proteins). The production, release, action and degradation of GABA at a stereotyped GABAergic synapseNeurons that produce GABA as their output are called GABAergic neurons, and have chiefly inhibitory action at receptors in the adult vertebrate. Medium Spiny Cells are a typical example of inhibitory CNS GABAergic cells. In contrast, GABA exhibits excitatory actions in insects, mediating muscle activation at synapses between nerves and muscle cells, and also the stimulation of certain glands. In mammals, some GABAergic neurons, such as chandelier cells, are also able to excite their glutamatergic counterparts.[2] GABA receptors are chloride channels; that is, when activated by GABA, they allow the flow of chloride ions across the membrane of the cell. Whether this chloride flow is excitatory/depolarizing (makes the voltage across the cell's membrane less negative), shunting (has no effect on the cell's membrane) or inhibitory/hyperpolarizing (makes the cell's membrane more negative) depends on the direction of the flow of chloride. When net chloride flows out of the cell, GABA is excitatory or depolarizing; when the net chloride flows into the cell, GABA is inhibitory or hyperpolarizing. When the net flow of chloride is close to zero, the action of GABA is shunting. Shunting inhibition has no direct effect on the membrane potential of the cell, however it minimises the effect of any coincident synaptic input essentially by reducing the electrical resistance of the cell's membrane (essentially equivalent to Ohm's law). A developmental switch in the molecular machinery controlling concentration of chloride inside the cell and hence the direction of this ion flow, is responsible for the changes in the functional role of GABA between the neonatal and adult stages. That is to say, GABA's role changes from excitatory to inhibitory as the brain develops into adulthood.[3] Structure and conformation GABA is found mostly as a zwitterion, that is, with the carboxy group deprotonated and the amino group protonated. Its conformation depends on its environment. In the gas phase, a highly folded conformation is strongly favored because of the electrostatic attraction between the two functional groups. The stabilization is about 50 kcal/mol, according to quantum chemistry calculations. In the solid state, a more extended conformation is found, with a trans conformation at the amino end and a gauche conformation at the carboxyl end. This is due to the packing interactions with the neighboring molecules. In solution, five different conformations, some folded and some extended are found as a result of solvation effects. The conformational flexibility of GABA is important for its biological function, as it has been found to bind to different receptors with different conformations. Many GABA analogues with pharmaceutical applications have more rigid structures in order to control the binding better. Synthesis Since GABA does not penetrate the blood brain barrier, GABA is therefore synthesized in vivo. It is synthesized from glutamate using the enzyme L-glutamic acid decarboxylase and pyridoxal phosphate (which is the active form of vitamin B6) as a cofactor via a metabolic pathway called the GABA shunt. This process converts glutamate, the principal excitatory neurotransmitter, into the principal inhibitory neurotransmitter (GABA) 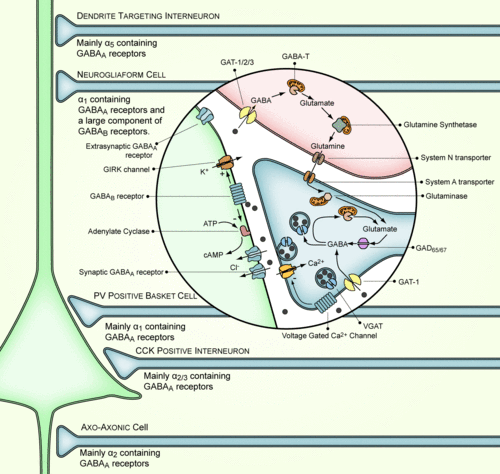  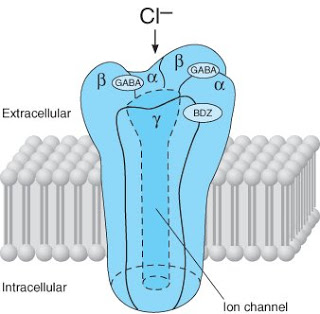 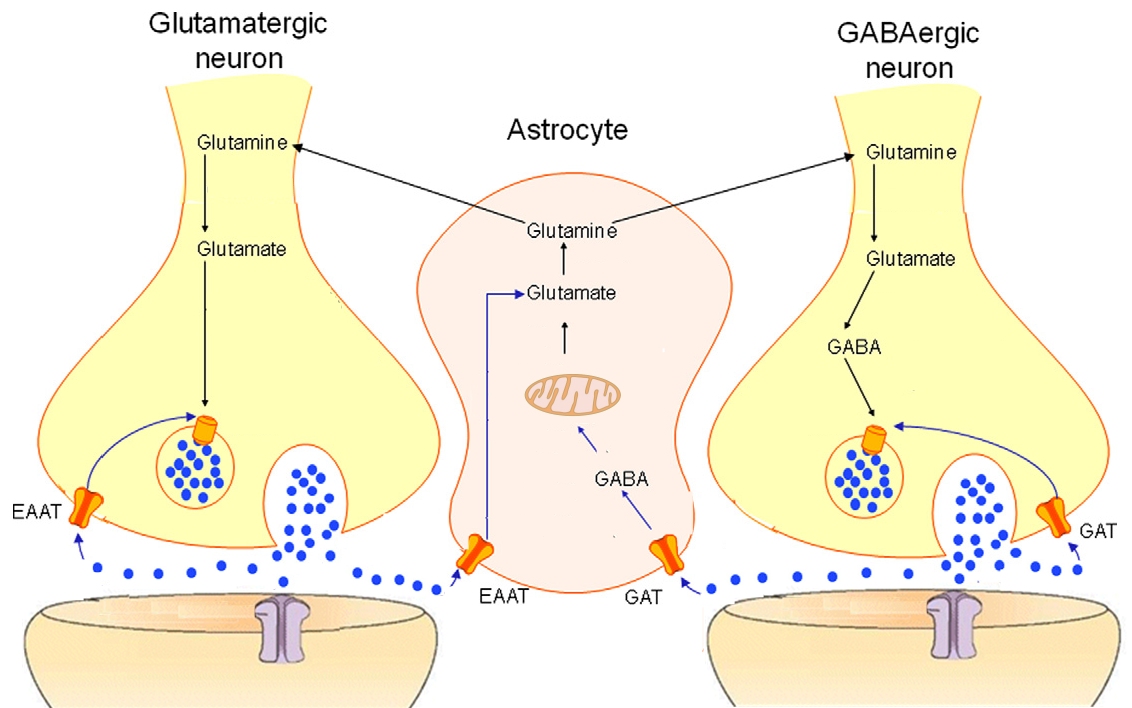 남궁 석 교수님 자료 뇌의 절반을 차지하지만 주목받지 못하던 별세포, 치매 치료의 새 길 연다 국내 연구진이 알츠하이머 치매 환자의 뇌 속 세포에서 기억력 감퇴를 유발하는 물질을 억제할 새로운 표적을 찾아냈다. 쥐를 이용한 동물실험에서 기억력을 회복할 수 있다는 사실까지 확인해 새로운 알츠하이머 치매 치료제 개발의 길이 열릴 것으로 기대된다. 이창준 기초과학연구원(IBS) 인지 및 사회성 연구단 단장과 류훈 한국과학기술연구원(KIST) 뇌과학연구소 신경과학연구단장 연구팀은 뇌에 있는 '별세포'에서 암모니아를 해독할 때 활용하는 요소회로의 존재를 확인하고 치매유발 물질이 이 회로의 활성화를 가속화해 기억력을 떨어뜨린다는 사실을 알아냈다고 23일 밝혔다. 별세포는 뇌를 구성하는 세포의 절반 이상을 차지하는 별 모양의 비신경세포다. 알츠하이머나 염증같은 주변 환경으로 별세포의 수와 크기가 증가하며 만들어지는 ‘반응성 별세포’는 주변 신경세포에 다양한 영향을 준다. 연구팀은 이번 연구에 앞서 반응성 별세포에서 만들어진 마오비(MAO-B) 효소가 단백질 부패성분인 푸트레신에서 억제성 신경전달물질 ‘가바(GABA)’를 만들어내 기억력을 감퇴시킨다는 사실을 알아냈다. 하지만 푸트레신이 어떻게 늘어나는지는 알지 못했다. 연구팀은 몸에 유해한 암모니아를 해독해 요소를 만드는 요소회로가 별세포에 존재하는 것을 확인하고 푸트레신과 요소회로가 연결되는 것을 알아냈다. 요소는 소변의 주성분으로 간에서 암모니아를 해독할 때 만들어져 신장을 통해 배출된다. 별세포에 알츠하이머 치매를 유발하는 독성물질인 '아밀로이드 베타'를 주입하자 요소회로를 작동하게 하는 효소인 OTC와 ARG1, ODC1의 활성과 발현량이 늘었다. 합성된 요소 양도 늘었다. 요소회로 활성화는 실제 알츠하이머 환자의 뇌 조직에서도 발견됐다. 연구팀은 요소회로에서 나온 ODC1이 푸트레신의 양을 늘리는 것을 발견했다. ODC1이 푸트레신을 늘리면 마오비 효소를 통해 가바로 전환되는 과정에서 암모니아가 다시 형성됐다. 이 암모니아가 다시 요소회로로 투입되면서 요소회로를 가동하면 다시 푸트레신이 늘어나고 또 암모니아가 늘어나는 증폭 현상이 발생하는 것을 확인했다. 베타 아밀로이드가 요소회로를 계속 돌리면 가바의 양이 늘어 기억력 감퇴로 이어진 것이다. 별세포에서 ODC1을 제거하자 푸트레신과 가바가 줄어드는 것뿐 아니라 알츠하이머 생쥐의 기억력이 회복되는 현상도 나타났다. ODC1을 끊어 암모니아가 늘어나는 걸 막아 푸트레신과 가바가 늘어나는 것도 막은 것이다. 여기에 ODC1이 줄어들면 아밀로이드 베타가 뭉치지 못하도록 하는 반응도 늘리는 것으로 나타났다. 아밀로이드 베타는 뭉칠수록 독성이 커지는데 이를 막는 효과도 나타난 것이다. 반응성 별세포에서 ODC1을 억제하면 치매를 치료할 수 있음을 보이면서 새로운 치매 치료 방법으로 활용될 것으로 기대된다. 지금까지는 알츠하이머 치매의 주원인으로 여겨진 아밀로이드 베타 자체를 제거하는 치료제들이 주로 개발돼왔다. 그러나 아밀로이드 베타를 제거해도 중증 치매가 계속되는 경우가 많아 치료제 개발에 난항을 겪고 있다. 지난해 미국 식품의약국(FDA) 허가를 받은 치매 치료제 ‘아두카누맙’도 아밀로이드 베타를 면역반응으로 제거하는 치료제지만 효능을 놓고 과학계 논란이 큰 상황이다. 류 단장은 “면역반응은 염증을 필연적으로 일으키는 만큼 염증이 원인이 되는 치매에 악영향을 줄 수 있다”고 말했다. 이번 연구를 통해 치매에 큰 영향을 미칠 것으로 예상했던 신경세포가 아닌 주변세포로 여겨졌던 별세포도 중요하다는 것이 확인됐다. 38년 전 뇌에서 암모니아가 발생하면 치매와 연관돼 있는 것을 밝혀냈지만 원인을 찾지 못했는데 그 원인도 밝혀냈다. 류 단장은 “반응성 별세포는 평소에는 신경세포에 도움을 주지만 임계값을 넘어가면 오히려 신경세포에 악영향을 미친다는 것을 밝혀냈다”며 “반응성 별세포의 역할에 초점을 맞추는 계기가 될 것”이라고 말했다. 신경세포와 달리 별세포는 뇌 연구에서 비주류로 여겨져 왔다. 그러나 한국은 별세포 분야에서 앞서나가는 만큼 별세포를 이용한 치료제 개발은 더욱 기회가 될 수 있다는 설명이다. 이 단장은 “치매의 원인을 복잡하다고 설명할 때는 잘 모르기 때문이라고 생각하는데, 기전을 정확하게 확인한 것 같다”고 말했다. 류 단장은 “한국에서 전 세계와 경쟁했을 때 별세포와 같은 특정 연구는 더 잘 도전할 수 있는 소재”라고 말했다. 연구팀은 요소회로와 가바를 만드는 과정에서 나오는 물질들을 공략해 새로운 치매 치료제를 개발하고 있다. 이 단장은 “새로운 치매 억제제 선도물질로 요소회로 효소의 ODC1 가능성을 확인했다”며 “전임상 시험을 통해 ODC1 효능과 독성을 확인하고 새 알츠하이머 치매 치료제 개발에 착수하면 7년 정도면 개발이 가능할 것”이라고 말했다. 연구팀은 2020년 별세포가 만드는 과산화수소가 치매를 유도하는 다른 원인임을 확인하고 과산화수소를 제거하는 치료제를 개발하는 임상 1상에도 착수한 상태다. 이번 연구에는 주연하 KIST 박사후연구원이 1저자로 참여했다. 연구 결과는 이달 23일 국제학술지 ‘셀 메타볼리즘’에 공개됐다. |
||||
|
|
|||